一方水土养一方人,一方人就得一方病。很多疾病都有着明显的集中分布区域,就连癌症也不例外,比如我国华南地区鼻咽癌的发病率,就是全世界平均水平的几十倍,因此中国医生治疗鼻咽癌的经验和水准,也走在全球前列。
毕竟求人不如求己,国内发病率这么高的癌症,中国医生当然要全力去攻克。而名头更大、致命程度更高的肝癌,在中国的患者人数则是鼻咽癌的好几倍,每年国内的新发病例数接近40万例,能够占到全球的一半以上。
对抗这么凶猛的敌人,就更需要“中国力量”站出来了。好在这个时代,有着能够扛起大旗的国产药物。PD-1抑制剂卡瑞利珠单抗在肝癌治疗领域,就已经交出了相当漂亮的答卷。
“以更少,做更多”
奇点糕们此前介绍过“网红艾瑞卡”的不少故事,卡瑞利珠单抗的网红名头,可是凭着实力赢得的。作为中国首个且唯一获批肝癌适应症的免疫检查点抑制剂,卡瑞利珠单抗的获批是基于一项登上《柳叶刀·肿瘤学》的临床II期研究。
这项临床II期研究由南京金陵医院秦叔逵教授和复旦大学中山医院任正刚教授共同牵头开展,是一项针对既往经过治疗的晚期肝细胞癌患者的多中心、开放性、平行、随机临床试验。
研究中卡瑞利珠单抗治疗的主要数据,让人眼前一亮:治疗的客观缓解率(ORR)为14.7%,其中仅接受过索拉非尼治疗的患者ORR更高,达到19.5%,患者的中位生存期(OS)为13.8个月,12个月生存率为55.9%。
与纳武利尤单抗(nivolumab)、帕博利珠单抗(pembrolizumab)等大名鼎鼎的国外PD-1抑制剂在肝癌二线治疗中的疗效相比,卡瑞利珠单抗的表现至少也达到了旗鼓相当,在客观缓解率方面甚至还小有优势[1-3]。
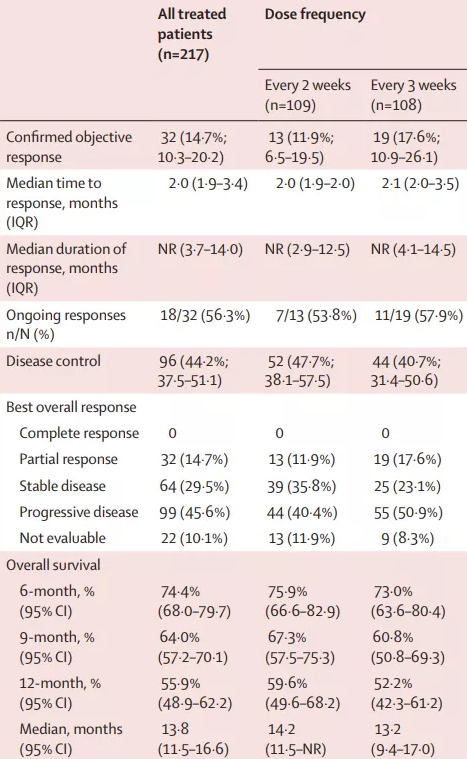
卡瑞利珠单抗II期试验的疗效数据
(图片来源:Lancet Oncology)
而且奇点糕有一句常说的话:看临床试验,不能只看疗效数据。仔细解读论文就能发现,卡瑞利珠单抗试验其实是在“入组患者基线水平相比同类研究更差,病情更复杂,恶性程度更高”的基础上,达到和国外PD-1抑制剂比肩的疗效。
“基线更差”,一方面体现在患者的不良预后因素更多。例如与帕博利珠单抗的II期试验相比,卡瑞利珠单抗试验入组的患者,有51%甲胎蛋白水平至少是400ng/ml,而帕博利珠单抗的试验中,只有41%的患者甲胎蛋白>200ng/ml。
而在巴塞罗那肝癌分期达到C级(95%对76%),ECOG评分为1分,提示患者身体条件基础较差(79%对39%)、肝外转移比例(82%对64%)等方面,卡瑞利珠单抗试验的患者状况也相对更差,不良预后的因素明显更多一些。
Do more with less,“以更少做更多”,用这句话概括卡瑞利珠单抗取得的疗效非常合适。“基线更差”的另一方面,则是卡瑞利珠单抗试验的入组患者,大多数是乙肝病毒(HBV)阳性,符合中国肝癌患者的现实情况。
卡瑞利珠单抗的临床II期试验共入组了217例患者,其中181例是HBV阳性,占比达到83%。而帕博利珠单抗的两项二线治疗试验中,HBV阳性的患者只有20-25%,纳武利尤单抗单药治疗试验的比例也差不多。
教科书上“中国和欧美国家肝癌存在很大差异”的说法,很大程度上就与HBV有关。正是因为这种差异,要指导中国的肝癌治疗临床实践,就必须基于来自中国人群的高级别循证医学证据。
如果免疫治疗试验入组的HBV阳性患者偏少,数据就不适合生搬硬套到国内。卡瑞利珠单抗的试验,则是首个针对中国HBV相关肝癌患者的大样本免疫治疗临床研究,也是目前全球范围内样本量最大的同类研究,无疑意义重大。

国外试验往往入组的丙肝患者较多,参考价值有限
(图片来源:Pixabay)
此外卡瑞利珠单抗的这项研究,也是首个登顶《柳叶刀·肿瘤学》的中国肝癌免疫治疗临床研究。中国医生和患者努力得到的循证医学证据,还推动了临床诊疗指南的更新。
2020版中国临床肿瘤学会(CSCO)肝癌诊疗指南中,卡瑞利珠单抗的二线治疗得到了I级专家推荐,可以说成为了二线治疗的新标准,也是属于中国人自己的治疗方案。
单枪匹马作战,卡瑞利珠单抗的表现已经备受认可。而在肝癌一线治疗的免疫联合方案大趋势中,卡瑞利珠单抗同样不落人后,表现抢眼。
“双艾组合”初现峥嵘
在所有实体肿瘤中,肝癌的凶险程度绝对排在前列,这与肝癌很强的免疫抑制性肿瘤微环境(TME)有着密切关系。让PD-1抑制剂单枪匹马,在一线治疗中实现破局,其实还是比较困难的[4]。

肝癌免疫微环境也是非常复杂的
(图片来源:Clinical Cancer Research)
因此目前PD-1/L1抑制剂们,大多在尝试联合方案冲击肝癌一线治疗,最常见的搭档是免疫+抗血管,比如帕博利珠单抗+仑伐替尼(lenvatinib)的组合,此外还有纳武利尤单抗+伊匹木单抗(ipilimumab)的双免疫,或者免疫+化疗等。
联合治疗的临床III期试验,一下子就铺开了十多项,可谓是你争我夺、战火激烈了。而在这种大趋势下,卡瑞利珠单抗不仅不落人后,甚至还“双线操作”,同时走了免疫+抗血管和免疫+化疗两条路。就先从免疫+抗血管的“双艾组合”,也就是卡瑞利珠单抗+阿帕替尼(商品名:艾坦)说起吧。
2018年的美国临床肿瘤学会(ASCO)年会上,卡瑞利珠单抗+阿帕替尼组合治疗肝癌、胃癌和胃食管连接癌的临床I期试验数据,以壁报的形式发布。
接受双艾组合治疗的16例肝癌患者,有8例达到了部分缓解,客观缓解率(ORR)和疾病控制率(DCR)分别为50%和93.8%,中位OS则尚未达到。
50%的客观缓解率让人眼前一亮,而且值得注意的是,研究入组的肝癌患者是此前接受过索拉非尼一线治疗,但疗效不佳或不能耐受的难治性患者,这就更加体现了双艾组合的疗效[6]。
基于这一结果,最新版的CSCO肝癌指南中,在一线治疗和二线治疗中同时推荐了卡瑞利珠单抗+阿帕替尼的组合。
“双艾组合”中的阿帕替尼,最近还交出了另外一份亮眼的答卷:2020年ASCO年会上公布的数据显示,阿帕替尼在临床III期的AHELP试验中,单药二线治疗明显优于安慰剂,患者的中位生存期为8.7个月,死亡风险相对下降了21%[5]。
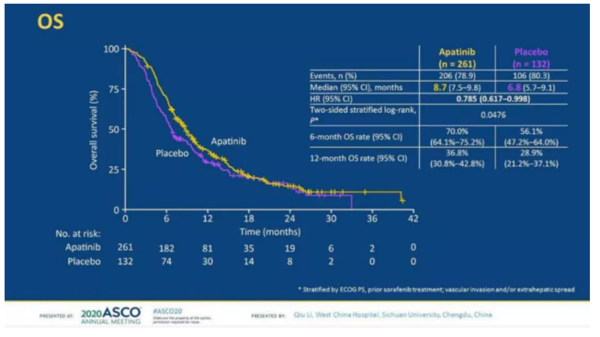
AHELP试验主要终点数据
(图片来源:2020 ASCO)
卡瑞利珠单抗+阿帕替尼的“双艾组合”,在小样本试验中的疗效出色,因此它们的大样本试验结果就颇受期待。
据奇点糕了解,由解放军总医院第五医学中心徐建明教授牵头开展,双艾组合治疗晚期肝细胞癌的II期RESCUE研究也已完成,相关数据即将公布。RESCUE研究入组了190例中国患者,也是免疫联合治疗试验中目前入组中国患者最多的试验。
与此同时,南京金陵医院秦叔逵教授与哈佛大学附属麻省总医院Andrew Zhu教授联合牵头开展的,卡瑞利珠单抗联合阿帕替尼对比索拉非尼,一线治疗晚期肝细胞癌的国际多中心Ⅲ期试验正在进行之中,这也是对“双艾组合”的终极考验,结果值得期待。
良好的表现,不只有一种体现方式
在联合化疗方面,卡瑞利珠单抗也取得了不小的进展。2019年ASCO年会上公布的数据显示,卡瑞利珠单抗联合FOLFOX4或GEMOX(吉西他滨+奥沙利铂)方案一线治疗时,ORR和DCR分别是26.5%和79.4%,患者中位PFS为5.5个月[7]。
不管是联合抗血管生成药物还是化疗,卡瑞利珠单抗的表现都相当不错,优秀的表现,还是要追溯到它的药物特点上。中山大学肿瘤防治中心的李苏教授,对卡瑞利珠单抗的临床药理特性进行了点评(以下有文字版要点):
“目前可及的PD-1各抗体药物虽同属于IgG4亚型,其人源化水平、结合位点以及活性并不相同。卡瑞利珠单抗是一种人源化的IgG4单克隆抗体,无ADCC、ADCP和CDC作用,从而有效降低了T细胞耗竭,有助于发挥持续抑瘤作用。”
“卡瑞利珠单抗具有独特的PD-1结合表位,在体内受体占有率高,在第22天仍大于95%;其IC50、EC50更低,分别为0.70nM和0.38nM,促进T细胞释放IFNγ能力更强。”
“与“温和型”抗体相比,卡瑞利珠单抗是一种‘独特而强效’的PD-1单抗,在淋巴瘤、肝癌、肺癌、食管癌等不同瘤种中均显示出疗效。此外,卡瑞利珠单抗在体内分布适当,半衰期较短,仅5.5天,可实现药物的快速清除,安全性、耐受性更好,这为免疫相关不良反应的管理带来了便利。”
此外近期一项对现有PD-1/L1抑制剂临床试验数据的Meta分析显示,PD-1抑制剂的整体疗效,可能略优于PD-L1抑制剂(OS HR 0.75, PFS HR 0.73)[8]。但具体到不同癌种的疗效,PD-1/L1抑制剂仍有一定差异,需要具体分析数据。
作为覆盖适应症最多的国产PD-1抑制剂,2020年上半年,卡瑞利珠单抗接连拿下了肝癌、肺癌、食管癌三大适应症。加上2019年获批的霍奇金淋巴瘤适应症,卡瑞利珠单抗已经拥有四大适应症。
那么在肝癌治疗上,卡瑞利珠单抗能不能上演“后来者居上”的好戏呢?不管是联合抗血管生成药物还是化疗,奇点糕都期待着更好更漂亮的临床试验结果,也希望卡瑞利珠单抗这个“中国力量”,能为中国肝癌患者带来更多获益。
参考资料:
1.Qin S, Ren Z, Meng Z, et al. Camrelizumab in patients with previously treated advanced hepatocellular carcinoma: a multicentre, open-label, parallel-group, randomised, phase 2 trial[J]. The Lancet Oncology, 2020, 21(4): 571-580.
2.Zhu A X, Finn R S, Edeline J, et al. Pembrolizumab in patients with advanced hepatocellular carcinoma previously treated with sorafenib (KEYNOTE-224): a non-randomised, open-label phase 2 trial[J]. The Lancet Oncology, 2018, 19(7): 940-952.
3.Finn R S, Ryoo B, Merle P, et al. Pembrolizumab As Second-Line Therapy in Patients With Advanced Hepatocellular Carcinoma in KEYNOTE-240: A Randomized, Double-Blind, Phase III Trial[J]. Journal of Clinical Oncology, 2020, 38(3): 193-202.
4.Yau T, Park J W, Finn R S, et al. CheckMate 459: A randomized, multi-center phase III study of nivolumab (NIVO) vs sorafenib (SOR) as first-line (1L) treatment in patients (pts) with advanced hepatocellular carcinoma (aHCC)[J]. Annals of Oncology, 2019, 30: v874-v875.
5.Li Q, Qin S, Gu S, et al. Apatinib as second-line therapy in Chinese patients with advanced hepatocellular carcinoma: A randomized, placebo-controlled, double-blind, phase III study [J]. Journal of Clinical Oncology, 2020, 38(15_suppl): 4507.
6.Xu J, Zhang Y, Jia R, et al. Anti-PD-1 antibody SHR-1210 combined with apatinib for advanced hepatocellular carcinoma, gastric, or esophagogastric junction cancer: an open-label, dose escalation and expansion study[J]. Clinical Cancer Research, 2019, 25(2): 515-523.
7.Xu J-M, Zhang Y, Jia R, et al. Anti-programmed death-1 antibody SHR-1210 (S) combined with apatinib (A) for advanced hepatocellular carcinoma (HCC), gastric cancer (GC) or esophagogastric junction (EGJ) cancer refractory to standard therapy: A phase 1 trial [J]. Journal of Clinical Oncology, 2018, 36(15_suppl): 4075.
8.Duan J, Cui L, Zhao X, et al. Use of immunotherapy with programmed cell death 1 vs programmed cell death ligand 1 inhibitors in patients with cancer: a systematic review and meta-analysis[J]. JAMA Oncology, 2020, 6(3): 375-384.
来源:奇点糕、本文作者 | 谭硕
健康资讯
- 肠癌常被误认为痔疮?康立明长安心让你摆脱肠癌风
- 卡瑞利珠单抗与阿帕替尼的“双艾组合”,有望改写
- 卡瑞利珠单抗与阿帕替尼的“双艾组合”,有望改写
- 大湾区智慧医疗加速度:科大讯飞牵手琶洲实验室共
- 上海海华医院AAA信用、五星级医院揭牌仪式暨建院五
- 壹步网:“国际残疾人日”正式上线,迈出无障碍生
- 苏丽萍教授、沈志祥教授解析硫培非格司亭在血液领
- 湘潭市中心医院呼吸与危重症医学科揭秘“起死回生
- 一位妈妈的悔恨:孕期没查甲状腺,生出智力有问题
- 女性最常见的几种癌症,该如何预防?
- 第三个国产PD-1单抗获批,这次是来自恒瑞
- 时时养小麦胚芽荣获“百项科普新产品”荣誉称号
- SNN:DFC靶向辅助治疗AD症状 实验证明可降低28%死亡率
- 宁波海曙协爱中医医院精神科特邀专家——冯永铭个
- 2020联合国糖尿病日主题活动圆满结束